Le silicium et ses composés. Silicon dans la nature. L'utilisation de silicium
L'un des plus populaires dans l'art et de l'industrie des éléments est le silicium. Qu'il doit ses propriétés inhabituelles. Aujourd'hui, il y a beaucoup de différents composés de cet élément, qui jouent un rôle important dans la synthèse et à la création de produits techniques, verrerie, verre, matériel, matériaux de construction, des bijoux et d'autres industries.

Caractéristiques générales de silicium
Si l'on considère la position du silicium dans le système périodique, il est possible de dire:
- IV est situé dans les principaux sous-groupes du groupe.
- Le numéro de séquence 14.
- masse atomique 28,086.
- Le symbole chimique Si.
- Nom – silicium, ou en latin – Silicium.
- La configuration électronique de la couche externe 4E: 2e: 8e.
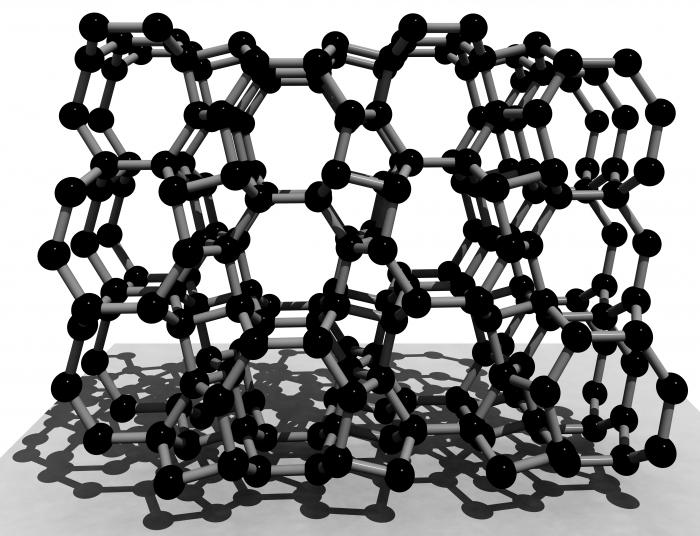
Le réseau cristallin de silicium est similaire au réseau de diamant. Les noeuds sont agencés atomes, son type – une cubique à faces centrées. Cependant, en raison de la plus grande longueur des propriétés physiques de communication de silicium diffèrent fortement des propriétés de modification allotropique de carbone.
Propriétés physiques et chimiques
Il y a deux modification allotropique de l'élément: amorphe et cristallin. Ils sont très similaires. Cependant, comme cela est le cas avec d'autres matériaux, la différence principale entre eux – le réseau de silicium cristallin.
Dans ce cas, les deux versions – une poudre de différentes couleurs.
1. silicium cristallin est un métal en forme de poudre gris foncé brillant. Sa structure correspond au diamant, mais des propriétés différentes. Il a:
- fragilité;
- faible dureté;
- propriétés semi-conductrices;
- La température de fusion de 1415 0 C;
- densité 2,33 g / cm 3;
- la température d' ébullition de 2700 0 C.
Son activité chimique est faible par rapport à une autre forme allotropique.
2. Le silicium amorphe – poudre brun brun, a la structure diamant silnorazuporyadochennogo. La réactivité est assez élevé.
D'une manière générale, il convient de noter que réagir dégoûts de silicium. Pour le faire réagir, la température nécessaire au moins 400-500 0 C. Divers composés chimiques sont formés de silicium dans ces conditions. Tels que:
- oxydes;
- des halogénures;
- suicides;
- nitrures;
- borures;
- carbures.
Peut-être l'interaction de silicium avec de l'acide nitrique ou un alcali, que l'on appelle un processus de gravure. silicones largement répandues, qui sont de plus en plus fréquents aujourd'hui.
Être dans la nature
Le silicium est naturellement présent dans une quantité assez importante. Il est à la deuxième place après la prévalence de l'oxygène. Sa fraction de poids est d'environ 30%. L'eau de mer contient également un élément actif à une concentration de 3 mg / L. Par conséquent, nous ne pouvons pas dire que le silicium dans la nature – il est un élément rare.
Au contraire, il y a beaucoup de roches et de minéraux différents, dans le cadre duquel il se produit et dont il peut être extrait. Les composés de silicium naturel les plus courants sont les suivants:
- Silice. La formule chimique SiO 2. Il y a toute une variété de formes de minéraux et de roches sur sa base: le sable, le silex, feldspath, quartz, cristal de roche, améthyste, calcédoine, cornaline, opale, jaspe et autres.
- Des silicates et des silicates d'aluminium. Le kaolin, le feldspath, le mica, les sels d'acide silicique, l'amiante, le talc.
Ainsi, la diffusion largement dans le silicium de la nature et ses composés sont très populaires et la demande pour les personnes à utiliser à des fins techniques.

Le silicium et ses composés
Étant donné que pur élément considéré exister ne peut donc avoir une importance différente de ses composés. Du point de vue chimique, il peut être trois état d'oxydation +2, +4, -4. Partant de cela, et aussi en raison de leur inertie, mais surtout à la structure du réseau cristallin, il génère les types de substances suivants:
- composés binaires avec les non-métaux (silane, un carbure, un nitrure, un phosphure, et ainsi de suite;
- oxydes;
- l'acide silicique;
- des silicates de métaux.
Considérons l'importance du silicium et ses composés, sont le plus courant et populaire pour les gens.

des oxydes de silicium
Il existe deux types de substances exprimées par la formule:
- SiO;
- SiO 2.
Cependant, le plus largement utilisé a le dioxyde. Il existe dans la nature sous la forme d'une très belle pierres semi-précieuses:
- agate;
- calcédoine;
- opale;
- cornaline;
- jaspe;
- améthyste;
- strass.
L'utilisation du silicium sous cette forme a trouvé son application dans la fabrication de bijoux. Incroyablement belle or et bijoux en argent faits avec ces semi – précieuses et des pierres semi – précieuses.
Quelques variations de la silice:
- quartz;
- rivière et sable de quartz ;
- silex;
- feldspaths.
L'utilisation de silicium dans ces types mis en œuvre dans la construction, l'ingénierie, l'électronique, l'industrie chimique, la métallurgie. Ensemble, les oxydes se rapportent à une énumérés seule substance – silice.
Karbid Kremniya et son utilisation
Silicium et ses composés – un matériau de l'avenir et le présent. Un tel matériau est du carbure de silicium ou carbure de l'élément. La formule chimique de SiC. Il se produit dans la nature comme moissanite minérale.
En pur sous forme de carbone et un composé de silicium – est beau, cristaux transparents, la structure de type diamant. Toutefois, à des fins techniques utilisés dans le matériel peint de couleur vert et noir.
Principales caractéristiques de la substance, ce qui permet son utilisation dans l'industrie, la technologie, l'industrie chimique, les éléments suivants:
- semiconducteur à large intervalle;
- très haute résistance (7 échelle de Mohs) ;
- résistant aux hautes températures;
- excellente elektroustoychivost et la conductivité thermique.
Tout cela permet l'utilisation de carbure de silicium comme matériau abrasif dans la métallurgie et la synthèse chimique. De plus, elle est basée LED produisent un large spectre d'action, des parties au four à verre, des buses, des torches, des bijoux (moissanite appréciés FIANITE ci-dessus).

Silane et sa signification
composé de silicium est un silane de l'hydrogène ainsi que le nom ne peut être obtenu par synthèse directe à partir de matières de départ. Pour obtenir les différents siliciures métalliques sont utilisés, qui sont soumis à un traitement acide. En conséquence, le gaz de silane est libéré et forme un sel de métal.
Il est intéressant de noter que le composé en question n'a jamais produit seul. Toujours dans la réaction d'un mélange de mono-, di- et trisilane dans lesquels les atomes de silicium sont reliés entre eux dans les chaînes.
Sur les propriétés de ces composés – agents réducteurs forts. Eux-mêmes ainsi facilement oxydables par l'oxygène, parfois explosive. Réaction violente avec toujours avec les halogènes beaucoup de dégagement d'énergie.
L'application des silanes suivants:
- Les réactions de synthèse organique, à la suite de laquelle il est important de silicones – silicone, le caoutchouc, les produits d'étanchéité, des lubrifiants, des emulsions et autres.
- Microelectronics (moniteurs LCD, schémas techniques intégrés, etc.).
- silicium polycristallin de haute pureté.
- prothèses dentaires.
Ainsi, les silanes dans le monde moderne est élevé.

L'acide silicique et silicates
Hydroxyde de l'élément – ils sont différentes silices. distinguées:
- méta;
- o;
- silicium polycristallin et d'autres acides.
Ils ont tous des caractéristiques communes – le déséquilibre extrême à l'état libre. Ils sont facilement décomposées par la chaleur. Dans des conditions normales, il y a de courte durée, tourner d'abord dans un sol, puis un gel. Après séchage, les gels de silice, de telles structures sont appelées. Ils sont utilisés comme adsorbants dans les filtres.
Important du point de vue de l'industrie, sont les sels d'acides siliciques – silicates. Ils sont à la base de la préparation de ces substances, telles que:
- verre;
- béton;
- ciment;
- zéolite;
- kaolin;
- porcelaine;
- en terre cuite;
- cristal;
- la céramique.
silicates de métaux alcalins – solubles, le reste – pas. Par conséquent, le silicate de sodium et de potassium est appelé verre soluble. adhésif de papeterie normale – ce qui est le sel de sodium de l'acide silicique.
Mais les composés les plus intéressants sont tous du même verre. Ce qui seules options pour cette substance aucune idée! Aujourd'hui, compte tenu de couleurs, optique, options de mat. La verrerie est surprenante dans sa splendeur et sa diversité. Lors de l'ajout certains oxydes métalliques et non métalliques dans le mélange peut obtenir une grande variété de types de verre. Parfois, même la même composition, mais différents pourcentages de composants conduit à une différence dans les propriétés de la substance. Des exemples sont la porcelaine et la terre cuite, qui formule SiO 2 * Al 2 O 3 K 2 O.
Le verre de quartz – est une forme de produit de grande pureté, dont la composition est décrite comme la silice.

dans les composés de silicium Discovery
Au cours des dernières années, des études ont montré que le silicium et ses composés – les participants les plus importants dans l'état normal des organismes vivants. la carence en C ou un excès de maladies associées à un élément donné tel que:
- le cancer;
- la tuberculose;
- l'arthrite;
- la cataracte;
- la lèpre;
- la dysenterie;
- rhumatismes;
- l'hépatite et d'autres.
les processus de vieillissement se sont également associés à la teneur quantitative du silicium. De nombreuses expériences sur les mammifères ont montré que l'absence d'un élément ayant des crises cardiaques, accidents vasculaires cérébraux, le cancer et le virus de l'hépatite C est activée.















