Au cœur de presque tous les moteur thermique est un phénomène thermodynamique que le travail effectué par le gaz lors de l'expansion ou la contraction. Il vaut la peine de se rappeler que la physique au travail fait référence à une mesure quantitative, qui caractérise l'action de certaines forces sur le corps. Conformément au gaz de travail, une condition préalable à la réalisation de ce qui est de changer son volume, il n'y a rien que le produit de la pression de ce changement de volume.

travail de gaz au changement de son volume peut être à la fois le caractère isobares et isothermes. De plus, le processus d'expansion réelle peut être, et arbitraire. travaux de gaz qui se fait en expansion isobarique, se trouve par la formule suivante:
A = pΔV,
dans lequel p – caractéristique quantitative de la pression du gaz, et AV – différence entre le volume initial et final.
Procédé selon l'une expansion du gaz dans la physique habituellement représenté sous la forme d'une séquence de l'individu le processus isobare et isochore. Ces derniers sont caractérisés en ce que le gaz de travail en tant que ses indices quantitatifs est nul car il n'y a pas de mouvement du piston dans le cylindre. Dans ces conditions, il apparaît que le gaz de travail à un processus arbitraire varie en proportion directe avec l'augmentation du volume du récipient, dans lequel le mouvement du piston.
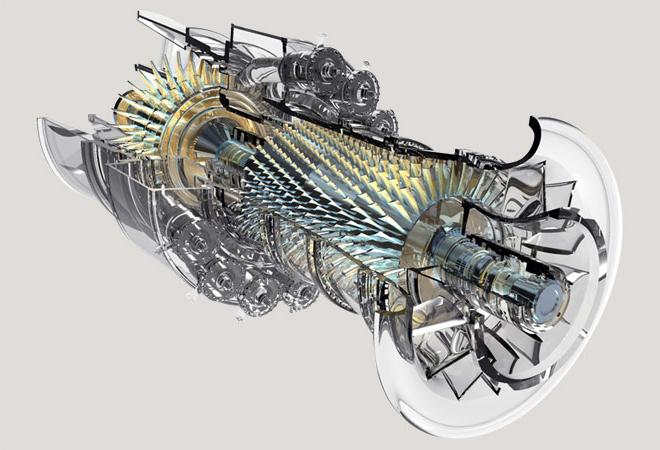
Si l' on compare le travail effectué par le gaz au cours de l' expansion et de la compression, il convient de noter qu'au cours de la direction d'extension du vecteur déplacement du piston coïncide avec le vecteur de la force de pression de ce gaz lui-même, mais dans le gaz de travail de calcul scalaire est positif et de forces extérieures – négatives. Lorsque le gaz comprimé sous la direction générale de déplacement du cylindre a la même vecteur de force externe, de sorte que leur travail est du gaz de travail positif et négatif.
Examen du concept de « travail accompli par le gaz » serait incomplète si elle n'a pas aussi affecter les processus adiabatiques. Dans un tel phénomène dans la thermodynamique se réfère au processus dans lequel il n'y a pas d'échange de chaleur avec des organismes externes. 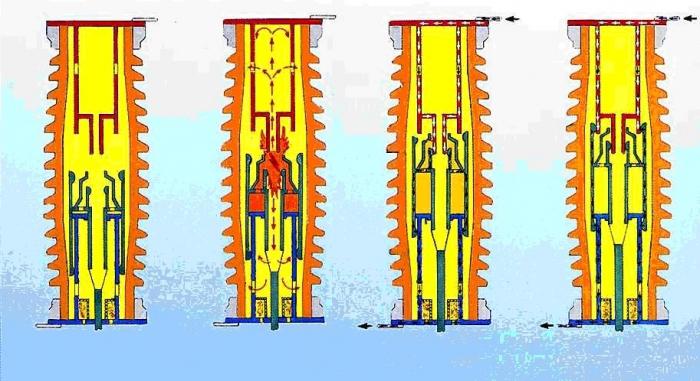 Il est possible, par exemple, dans le cas où un navire avec un piston de travail est doté d'une bonne isolation thermique. En outre, la compression du gaz ou des procédés d'extension peuvent être assimilés à adiabatique si les changements de temps dans le volume de gaz est nettement inférieure à l'intervalle de temps pendant lequel l'équilibre thermique se produit entre le gaz et les organes environnants.
Il est possible, par exemple, dans le cas où un navire avec un piston de travail est doté d'une bonne isolation thermique. En outre, la compression du gaz ou des procédés d'extension peuvent être assimilés à adiabatique si les changements de temps dans le volume de gaz est nettement inférieure à l'intervalle de temps pendant lequel l'équilibre thermique se produit entre le gaz et les organes environnants.
Le plus souvent rencontrées dans le processus de la vie quotidienne adiabatiques peut être considéré comme le travail du piston dans le moteur à combustion interne. L'essence de ce processus est le suivant: comme nous le savons de la première loi de la thermodynamique, la variation de l'énergie interne du gaz est quantitativement égale à la force de travail, dirigé de l' extérieur. Ce travail est dans sa direction est positive, et donc l'énergie interne du gaz augmentera, et la montée de la température de lui – même. Dans de telles conditions initiales, il est clair que, dans le travail d'expansion des gaz adiabatique se produira en raison de la réduction de son énergie interne, respectivement, la température dans ce processus va diminuer.









