Afin d'établir la composition qualitative de nombreux aliments utilisés réaction ksantoproteinovaya à la protéine. La présence d'acides aminés aromatiques dans le mélange va changer dans un échantillon de test positif couleur.
Qu'est-ce que la protéine
Il est aussi appelé une protéine, qui est un matériau de construction pour le corps vivant. Les protéines maintiennent la taille des muscles, restaurer les structures de tissus blessés et les morts de divers organes, que ce soit les cheveux, la peau et les ligaments. Avec leur participation, produit des globules rouges, est régie par le fonctionnement normal de nombreuses hormones et les cellules du système immunitaire. 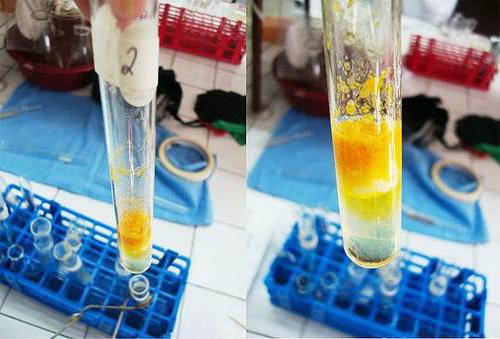
Ceci est une molécule complexe qui est un polypeptide ayant une masse supérieure à 6 ~ 10 3 daltons. La structure des protéines formant des résidus d'acides aminés dans un grand nombre de liaisons peptidiques couplées.
La structure des protéines
La particularité de ces substances par rapport aux peptides de faible poids moléculaire est qu'ils ont développé une structure spatiale en trois dimensions, supportés effets avec des degrés variables d'attraction. Les protéines possèdent la structure à quatre. Pour chacun d'eux a ses propres caractéristiques.
Comme la base de l'organisation primaire des molécules dérivées séquence d'acides aminés, la structure qui reconnaît réaction de ksantoproteinovaya à la protéine. Cette structure est un radical partie sélective liaison peptidique se répétant périodiquement -HN-CH-CO-, sont les chaînes latérales en acides aminés. Ils définissent d'autres propriétés de la substance dans son ensemble.
La structure primaire de protéine est considérée comme assez forte, cela est dû à la présence d'interactions covalentes fortes dans des liaisons peptidiques. La formation de niveaux subséquents se produit en fonction des attributs définis dans l'étape initiale.
La formation de la structure secondaire est possible en raison de la torsion de la séquence d'acides aminés dans une spirale, dans laquelle des liaisons hydrogène sont établies entre les spires.
organisation de niveau supérieur de molécules formé par application d'une d'une spirale sur les autres fragments de l'apparition de toutes les connexions possibles entre eux, avec de l'hydrogène, disulfure, covalent ou composé ionique. Le résultat est l'association sous la forme de globules. 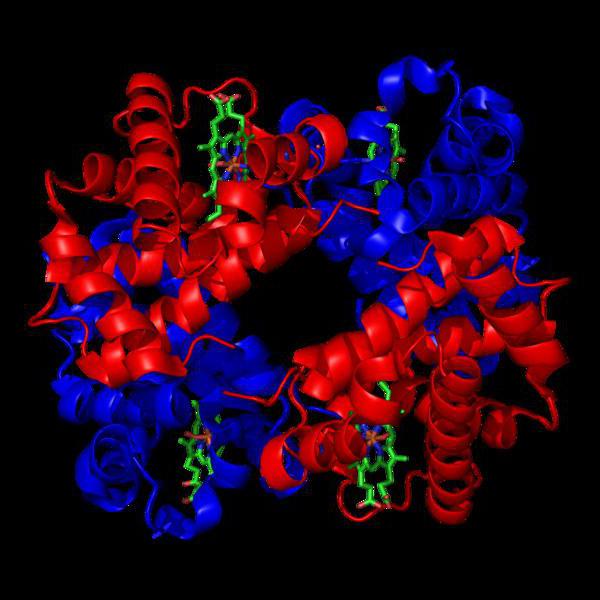
La disposition spatiale des structures tertiaires avec la formation de liaisons chimiques entre les conduit à la formation de la forme finale de la molécule ou des niveaux quaternaire.
Les acides aminés
Ils provoquent les propriétés chimiques des protéines. Il y a environ 20 acides aminés principaux constituant les polypeptides dans un ordre différent. Cet acide aminocarboxylique est également désigné rare sous la forme hydroxyproline et hydroxylysine dérivé peptidique basique.
En signe de reconnaissance de protéine de réaction ksantoproteinovaya, la présence de certains acides aminés fournit le changement de couleur des réactifs, ce qui suggère la présence de structures spécifiques dans leur composition.
En fin de compte, ils sont des acides carboxyliques qui se sont produits de substitution d'atome d'hydrogène sur le groupe amino.
Un exemple de structure de la molécule peut servir une formule structurelle glycine (HNH- HCH COOH) sous forme d'acide aminé simple. 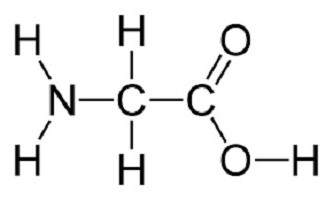
Dans ce cas , l' un des hydrogènes CH 2 – peuvent être remplacés par un atome de carbone radical comprenant plus d' un cycle benzénique, un groupe amino, sulfo, carboxy.
Qu'est-ce que la réaction de ksantoproteinovaya
Pour une analyse qualitative des protéines en utilisant diverses techniques. Ceux-ci comprennent des réactions:
- biuret avec l'apparition de couleur violette;
- ninhydrine pour former une solution bleu-violet;
- formaldéhyde avec la mise en place d'une couleur rouge;
- Nogier pour précipiter la couleur gris-noir.
Dans la réalisation de chaque procédé a prouvé la présence de protéines et la présence de certains groupes fonctionnels dans leur molécule.
Il ksantoproteinovaya réaction à la protéine. Il est aussi appelé la ventilation Mulder. Elle se réfère aux réactions colorées pour les protéines, dans lequel il y a des acides aminés aromatiques et hétérocycliques.
Une caractéristique d'un tel procédé d'échantillonnage est nitration nitrique acide résidus d'acide aminé cyclique , en particulier l'adhésion du groupe nitro en le noyau benzénique.
Le résultat de ce procédé est la formation de composés nitro, des précipités. Ceci est la réaction caractéristique de ksantoproteinovaya de base.
Ce qui a déterminé l'acide aminé
Ne peut pas être détectée tout aminocarboxylique en utilisant un tel échantillon. La caractéristique principale de la réaction de détection de la protéine ksantoproteinovaya – la présence du cycle benzène ou un cycle hétérocyclique dans la molécule d'acides aminés.
Étant donné que la protéine est isolée à partir d'acides aminocarboxyliques aromatiques deux, dans lequel il y a un groupe phényle (pour la phenylalanine), et un radical hydroxyphényle (en tyrosine). 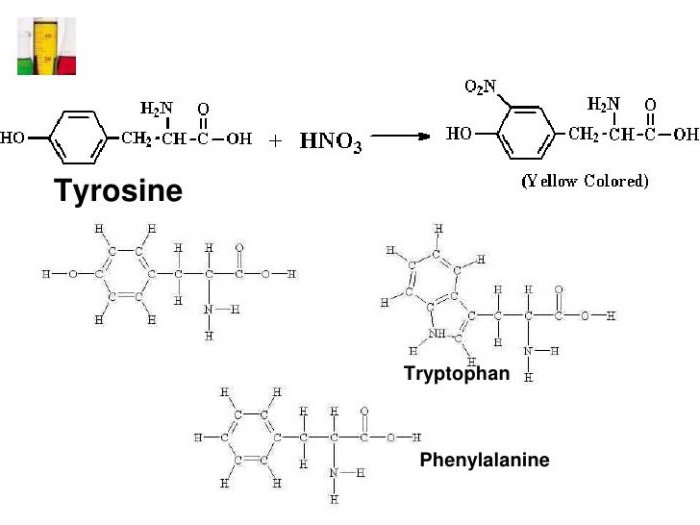
Avec la réaction de ksantoproteinovaya est déterminée tryptophane, un acide aminé hétérocyclique, de l'indole ayant un noyau aromatique. La présence des composés ci-dessus dans la protéine donne le changement de couleur caractéristique de l'environnement de test.
Qu'est-ce que l'utilisation des réactifs
Pour effectuer la réaction ksantoproteinovaya besoin pour préparer une solution à 1% de protéine d'oeuf, ou d'origine végétale.
Habituellement utilisé oeuf, qui est divisé par une séparation supplémentaire de la protéine du jaune d'oeuf. Pour une solution à 1% de protéine a été diluée dans une quantité décuple d'eau purifiée. Après dissolution du liquide de protéine résultante doit être filtré à travers plusieurs couches de gaze. Cette solution doit être stockée dans un endroit frais.
Il est possible de réaliser la réaction avec une protéine végétale. Pour préparer la solution est utilisée la farine de blé en une quantité de 0,04 kg. 0,16 l d'eau purifiée. Les ingrédients ont été mélangés dans un flacon qui est lié pendant 24 heures dans un endroit frais à une température d'environ + 1 ° C A la fin de la journée, la solution a été agitée, suivie d'une filtration de celui-ci d'abord avec de la laine de coton et ensuite – un filtre plissé en papier. Le liquide résultant a été maintenu dans un endroit frais. Cette solution est principalement présent dans la fraction d'albumine.
Pour mettre en oeuvre le ksantoproteinovaya de réaction comme réactif principal utilisé concentré d'acide nitrique. D'autres réactifs est une solution de 10% d'hydroxyde de sodium ou l'ammoniac, la solution de gélatine et de phénol non concentrée.
La méthodologie du
Dans un tube propre est faite 1% de solution de protéine d'oeufs -ième ou de la farine en une quantité de 2 ml. A cela on ajoute environ 9 gouttes d'acide nitrique concentré à floculation arrêté. On a chauffé le mélange obtenu, résultant précipité jaune disparaît peu à peu et sa couleur passe en solution. 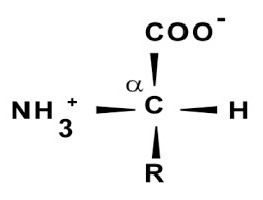
Lorsque le liquide se refroidit dans le tube le long de la paroi ajouté environ 9 gouttes d' hydroxyde de sodium, on concentre, ce qui est en excès du processus. Le milieu réactionnel devient alcalin. Contenu devient orange dans le tube à essai.
Caractéristiques de
Depuis ksantoproteinovaya appelé réaction qualitative à l' acide nitrique par l'action des protéines, l'échantillon est réalisée sous inclus hotte. Respectez toutes les consignes de sécurité lorsque l'on travaille avec des substances caustiques concentrées.
La libération du contenu du tube peut se produire pendant le processus de chauffage qui doit être considéré lors de la fixation dans un support et en sélectionnant l'inclinaison.
La numérotation de l'acide nitrique concentré et de la soude caustique ne doit en utilisant une pipette en verre et les poires pipette interdit de caoutchouc par la bouche.
réaction par rapport au phénol
Par souci de clarté, le processus et la confirmation de la présence des groupes phényle est réalisée avec un échantillon similaire hydroxybenzène.
Le tube faisant 2 ml de phénol dilué, puis progressivement le long de la paroi, on a ajouté 2 ml d'acide nitrique concentré. La solution a été soumise à un chauffage, de sorte qu'il devient jaune. Cette réaction est la qualité de la présence du noyau benzénique. 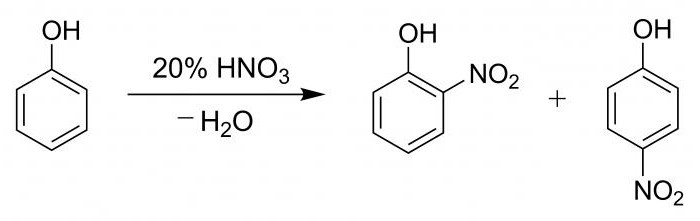
Procédé hydroxybenzène nitré avec de l'acide nitrique suivie de la formation d'un mélange de p-nitrophénol et o-nitrophénol dans un pourcentage de 15 à 35.
Test de comparaison avec la gélatine
Pour prouver que la réaction de ksantoproteinovaya à la protéine révèle un acide aminé avec une structure aromatique, utiliser des protéines qui ne possèdent pas un groupe phénolique.
Dans un tube propre est constitué de 1% de solution de gélatine en une quantité de 2 ml. A cela on ajoute environ 9 gouttes d'acide nitrique concentré. Le mélange résultant est chauffé. La solution n'a pas été coloré en jaune, ce qui prouve l'absence d'acides aminés avec une structure aromatique. Parfois, il y a un léger jaunissement de l'environnement en raison de la présence d'impuretés de protéines.
équations chimiques
Dans la réaction en deux étapes fonctionne ksantoproteinovaya protéines. Formule premier procédé de nitration de phase décrit des molécules d'acides aminés à l'aide d'acide nitrique concentré.
Un exemple est la fixation du groupe nitro en tyrosine pour former nitrotyrosine et dinitrotirozina. Dans le premier cas pour le noyau benzénique est fixé un NO 2 -radical, et le second composé possède deux atomes d'hydrogène sont remplacés par le NO 2. réaction de la tyrosine de formule chimique ksantoproteinovaya représenté par réaction avec l'acide nitrique pour former la molécule de nitrotyrosine.
Procédé de nitration est accompagné par une transition colorant incolore dans le ton jaune. Dans la réalisation de cette réaction avec des protéines contenant des résidus d'acides aminés phénylalanine ou le tryptophane, et la couleur de la solution change.
La deuxième étape est le produit de la réaction de nitration des molécules de tyrosine, en particulier nitrotyrosine, avec de l'ammonium ou de l'hydroxyde de sodium. Le résultat est un sel de sodium ou d'ammonium, dans lequel la couleur jaune-orange. Une telle réaction est liée à la possibilité de molécules de nitrotyrosine se déplacent sous la forme quinoïde. Par la suite le sel formé à partir de l'acide Nitronic, qui a un système quinone de doubles liaisons conjuguées. 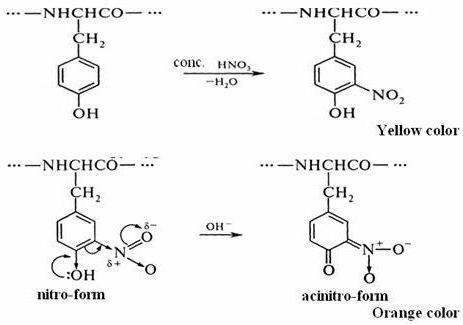
Ainsi se termine la réaction de ksantoproteinovaya aux protéines. L'équation ci-dessus présentée deuxième étape.
résultats
Lors de l'analyse de fluides contenus dans les trois tubes, la solution de référence est dilué avec du phénol. Les substances ayant un cycle benzène donnent réaction qualitative avec l'acide nitrique. En conséquence, il change de couleur de la solution.
Comme on le sait, la gélatine comprend une forme hydrolysée de collagène. La protéine ne contient pas la structure aromatique des acides aminés. Aucun changement de couleur du milieu de réaction avec un acide.
Dans le troisième tube à essai il y a une réaction positive aux protéines ksantoproteinovaya. Conclusion peut être tirée de la façon suivante: toutes les protéines ayant une structure aromatique, que ce soit un groupe phényle ou un cycle indole, compte tenu du changement de couleur de la solution. Ceci est dû à la formation de composés nitrés avec une couleur jaune.
La réalisation d'une réaction de coloration révèle la présence de diverses structures chimiques des acides aminés et des protéines. gélatine exemple montre que sa composition comprend de l'acide aminocarboxylique de ne pas avoir un groupe phényle ou une structure cyclique.
Avec ksantoproteinovaya réaction peut être expliqué par le jaunissement de la peau lorsqu'elle est appliquée à un fort acide nitrique. La même couleur deviendra le lait mousseuse au cours de son analyse similaire.
Dans la pratique de laboratoire clinique cet échantillon de couleur n'est pas utilisé pour la détection de protéines dans l'urine. Cela est dû à la couleur jaune de l'urine elle-même.
Ksantoproteinovaya réaction est devenu de plus en plus utilisé pour la quantification des acides aminés tels que le tryptophane et la tyrosine, dans le cadre de diverses protéines.












