les propriétés de l'ozone (élément chimique) de désignation de formule
Il est extrêmement précieux pour l'humanité tout entière les propriétés d'un gaz tel que l'ozone. Element, dont il est formé, – cet oxygène O. En fait, l' ozone O 3 – une oxygénation des modifications allotropiques constitué de trois unités de formular (O ÷ O ÷ G). Un premier et un composé connu – lui – même est de l' oxygène gazeux est précisément ce qu ' il est formé de deux atomes (D = O) – O 2. 
Allotropy – la capacité d'un élément chimique pour former un certain nombre de propriétés différentes de composés simples. Merci à l'humanité et l'utilisation de substances telles Examiné que le diamant et le graphite, le soufre monoclinique et orthorhombique, l'oxygène et l'ozone. Élément ayant une telle capacité n'est pas nécessairement limitée à seulement deux modifications, un peu plus d'entre eux.
Histoire des composés de découverte
L'unité de composant de nombreuses substances organiques et inorganiques, y compris tels que l'ozone – un élément chimique dont le symbole O – oxygène, dans «Oxys» grec – aigre et «gignomai» – pour donner naissance. 
Pour la première fois une nouvelle modification allotropique de l' oxygène au cours des expériences avec des décharges électriques découverts en 1785 le Néerlandais Martijn van Maron, son attention a été attirée odeur. Un siècle plus tard le Français Christian Friedrich Schönbein a noté la présence du même après une tempête, dans lequel le gaz a été nommé « sentir ». Mais certains scientifiques sont trompés, croyant que leur sens de l'odorat se parfumé à l'ozone. Odeur qu'ils se sentaient appartenaient composés organiques oxydés par réaction avec O 3, en tant que gaz est très réactif.
Structure électronique
Le même fragment structural sont O2 et O3 – un élément chimique. L'ozone a une structure plus complexe. L'oxygène est toujours simple, – deux atomes d'oxygène avec reliées par une double liaison et comprenant des composants π ϭ-, selon la valence de l'élément. Environ 3 a plusieurs structures de résonance.  liaison multiple reliant les deux atomes d'oxygène, et la troisième a une seule partie. Ainsi, en raison de composants de π migration, une image totale des trois atomes sont une seule et une connexion moitié. Cette relation est plus courte qu'une seule, mais plus que le double. La probabilité de molécules de récurrence scientifiques ont mené des expériences exclues.
liaison multiple reliant les deux atomes d'oxygène, et la troisième a une seule partie. Ainsi, en raison de composants de π migration, une image totale des trois atomes sont une seule et une connexion moitié. Cette relation est plus courte qu'une seule, mais plus que le double. La probabilité de molécules de récurrence scientifiques ont mené des expériences exclues.
méthodes de synthèse
Pour la formation d'un gaz tel que l'ozone, un élément chimique d'oxygène doit être dans un milieu gazeux sous la forme d'atomes individuels. De telles conditions sont créées dans la collision de molécules d'oxygène avec des électrons O 2 pendant les décharges électriques ou d' autres particules à haute énergie, et quand il est irradié avec de la lumière ultraviolette. 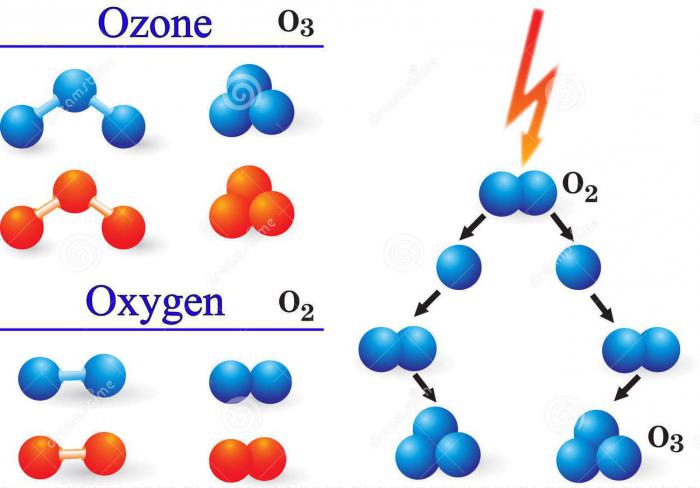
La part de la quantité totale d'ozone du lion produit par voie photochimiques dans les conditions atmosphériques naturelles. Les gens préfèrent utiliser l'activité chimique d'autres méthodes telles que, par exemple, la synthèse électrolytique. Elle consiste en ce que les électrodes de platine en milieu électrolyte aqueux placé et laissé en cours. Le schéma réactionnel:
H 2 O + O 2 → O 3 + H 2 + e –
propriétés physiques
L'oxygène (O) – composant unitaire comme substance d'ozone – élément chimique dont la formule et de la masse molaire relative sont indiqués dans le tableau périodique. La formation d' une O 3 avec de l' oxygène, elle acquiert les propriétés fondamentalement différentes de celles de O 2. 
bleu gaz – c'est un état commun de composés tels que l'ozone. Formule d'élément chimique caractéristiques quantitatives – tous définis dans l'identification et l'étude de la substance. Le point d'ébullition pour lui -111,9 ° C, état liquéfié a une couleur pourpre foncé, tout en réduisant encore le degré de -197,2 ° C fusion commence. Dans l'état solide de l'ozone d'agrégation devient couleur noire avec une teinte pourpre. Sa solubilité dix fois plus élevée que la propriété est de l'oxygène O 2. Lorsque les concentrations les plus faibles dans l'air l'odeur de l'ozone, il est forte, spécifique et ressemble à l'odeur du métal.
propriétés chimiques
Très actif, avec un point de vue de la réaction, le gaz est l'ozone. Élément chimique qu'il forme – est l'oxygène. Les caractéristiques qui déterminent le comportement de l'ozone dans l'interaction avec d'autres substances, – une grande capacité d'oxydation et de l'instabilité du gaz lui-même. A des températures élevées, il se décompose à une vitesse sans précédent, d' accélérer le processus et les catalyseurs tels que les oxydes métalliques, le dioxyde de chlore, l' azote et autres. propriétés oxydantes des caractéristiques structurelles inhérentes à l' ozone en raison de la mobilité de la molécule et une avec des atomes d'oxygène, qui clive se transforme en gaz oxygène: O 3 → O 2 + O ·
Oxygène (bloc de construction à partir de laquelle les substances moléculaires construits tels que l'oxygène et l'ozone) – élément chimique. Comme il est écrit dans les équations de réaction – A propos ·. L'ozone oxyde tous les métaux sauf l'or, le platine et ses sous-groupes. Il réagit avec les gaz dans l'atmosphère – les oxydes de soufre, d'azote et d'autres. Pas rester inertes et des substances organiques, en particulier des processus rapides sont des discontinuités des liaisons multiples par le biais de la formation de composés intermédiaires. Il est impératif que les produits de réaction sont inoffensifs pour l'environnement et les humains. Cette eau, l' oxygène, des oxydes supérieurs des différents éléments, les oxydes de carbone. La réaction avec l'ozone ne vient pas de composés binaires de calcium, de titane et de silicium avec de l'oxygène. 
application
La zone principale où utilisé « sentir » le gaz – il ozonation. Une telle méthode de stérilisation est beaucoup plus efficace et plus sûr pour les organismes vivants que la désinfection au chlore. Lors de la purification de l'eau avec formation d'ozone se produit des dérivés toxiques de méthane halogène dangereux substitués.
De plus en plus, cette méthode écologique de stérilisation est utilisée dans l'industrie alimentaire. Ozone traité avec des équipements de réfrigération, des installations de stockage pour les produits avec l'aide emmenez à l'élimination des odeurs.
Pour des propriétés désinfectantes médicaux d'ozone sont également indispensables. Ils désinfectent la plaie, des solutions salines. le sang veineux ozonée, ainsi que le gaz « sentir » traiter un certain nombre de maladies chroniques.
Être dans la nature et la valeur
ozone substance simple – élément région stratocaster composition de gaz à proximité de l'espace situé à une distance d'environ 20 à 30 km de la surface. L'isolement de ce composé se produit pendant les processus associés aux décharges électriques, pendant le soudage, l'appareil de copieur. Mais dans la stratosphère, il est formé et contient 99% de la quantité totale d'ozone présente dans l'atmosphère de la terre.
Vital a prouvé la présence de gaz dans l'espace proche de la Terre. Il se forme dans celle-ci une couche d'ozone que l'on appelle, qui protège toute la vie du rayonnement solaire ultraviolet létale. Curieusement, mais sur un pied d'égalité avec un énorme avantage, le gaz lui-même est dangereux pour les humains. L'augmentation de la concentration d'ozone dans la personne de respirer de l'air nocif pour l'organisme, en raison de sa réactivité extrême.