L'une des pierres d'achoppement dans les premières étapes de l'étude des lois chimiques et les fondations est d'écrire des réactions chimiques. Par conséquent, des questions sur l'interaction de CaCl2, H2SO4 trouvé pas périodiquement et systématiquement. Examinons les principaux moments de « problème ».
La fiche équation moléculaire
L'interaction entre le chlorure de calcium (sel) et l'acide sulfurique coule à travers le mécanisme d'échange.
 Maîtres mots de cette réaction sont:
Maîtres mots de cette réaction sont:
- deux connexions à l'entrée (matières premières);
- deux connexions à la sortie (produit);
- absence totale de substances simples.
Échanger des uns avec les autres groupes réactifs, les réactifs sont modifiés, et l'équation prend la forme:
CaCl2 + H2SO4 = CaSO4 + 2HCl.
Comme on le voit, deux substance complexe, des ions changeants former un composé très différents: un nouveau sel (CaSO4) et de l'acide chlorhydrique (HCl).
Pour circuler jusqu'à la fin
Répondre à cette question peut être simplement en écrivant à CaCl2, l'équation de réaction H2SO4 sous forme moléculaire. Le type de produits et tout dépendra. Jusqu'à la fin du processus est dans le cas de l'éducation:
- Matières solubles (boues);
- composé volatil (gaz);
- malodissotsiiruschego réactif (eau, électrolyte faible).
En contrepartie de cas CaCl2, H2SO4 là parmi les produits de réaction de sulfate de calcium – précipite composé faiblement soluble en fonction de la table.
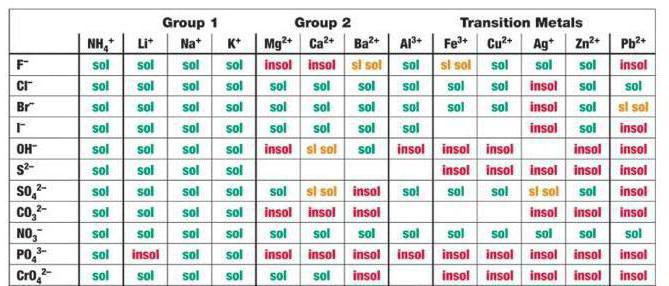
Par conséquent, le processus d'échange aura lieu jusqu'à la fin.
Résumées sous forme ionique entre l'enregistrement de CaCl2, H2SO4
En écrivant tous les composés solubles en ions et la réduction récurrente des groupes réactifs, on obtient deux équations à l'inconnu:
- complet enregistrement sous forme ionique entre CaCl2, H2SO4
Ca2 + 2cl – + 2H + + si 4 = 2- CaSO 4 + 2H + + 2cl –
- une forme raccourcie de l'équation
Ca2 + + SO 4 2- = CaSO 4.
Il faut se rappeler que seuls les ions peints sels solubles, acides, bases (ce qui est facilement déterminée à partir de tables spéciales). Faible carbonique de type électrolytes ou de l'acide acétique est toujours écrite sous la forme moléculaire.
Maintenant, vous savez comment l'interaction entre le chlorure de calcium (sel), et de l'acide sulfurique.