Nitration du toluène: équation de réaction
Parlons de la façon dont la nitration de toluène. De même préparé en faisant réagir un grand nombre de produits semi-finis utilisés dans la fabrication d'explosifs, de produits pharmaceutiques.
L'importance de nitration
des dérivés de benzène en tant que composés nitro aromatiques sont disponibles dans l'industrie chimique moderne. Nitrobenzene en aniline est un produit intermédiaire, le parfum, la production pharmaceutique. Il est excellent solvant pour un grand nombre de composés organiques, y compris la cellulose et de nitrite de former une masse gélatineuse avec lui. Dans l'industrie pétrolière, il est utilisé comme purificateur pour les huiles lubrifiantes. Lorsque la nitration de toluène est préparé benzidine, l'aniline, l'acide aminosalicylique, la phénylènediamine.

Caractéristiques de nitration
Nitration caractérisé groupe NO2 entrée dans la molécule du composé organique. En fonction du produit de départ, ce processus se déroule par un mécanisme radicalaire, nucléophile, électrophile. Les particules actives agissent en tant que cations, des ions nitronium et les radicaux NO2. réaction Toluène nitré fait référence au remplacement. Pour d'autres substances organiques peuvent substitution nitration, et l'addition de la double liaison.
Nitration du toluène dans une molécule de l'hydrocarbure aromatique est effectuée en utilisant un mélange sulfonitrique (acides sulfurique et nitrique). Le catalyseur présente des propriétés de l'acide sulfurique servant de moyens de traitement vodotnimayuschego.
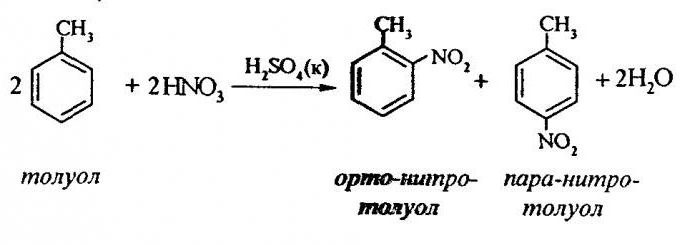
équation de processus
Nitration du toluène implique la substitution d'un atome d'hydrogène par un groupe nitro. Comment le schéma du processus en cours?
Afin de décrire la nitration du toluène, l'équation de la réaction peut être représentée comme suit:
ArH + HONO2 + = Ar-NO2 + H2 O
Il vous permet d'être jugé que sur le cours général de l'interaction, mais ne divulgue pas toutes les fonctionnalités de ce processus. En fait, il y a une réaction entre les hydrocarbures aromatiques et les produits de l'acide nitrique.
Étant donné que le produit a une molécule d'eau, on réduit la concentration de l'acide nitrique, nitration du toluène par conséquent, ralentit. Afin d'éviter ce problème, le procédé est réalisé à basse température en utilisant l'acide nitrique en une quantité en excès.
L' addition de l' acide sulfurique comme agents déshydratants utilisés , l' anhydride acétique, l' acide polyphosphorique, le trifluorure de bore. Ils permettent snizat la consommation d'acide nitrique, d'augmenter l'efficacité de l'interaction.

Les nuances du processus
La nitration du toluène a été décrit à la fin du XIXe siècle V. Markovnikov. Il a été en mesure d'établir un lien entre la présence dans le mélange réactionnel d' acide sulfurique concentré et le débit d'écoulement de processus. Dans nitrotoluène de production moderne acide nitrique anhydre sont utilisés, pris en léger excès.
En outre, la sulfonation et de nitration de toluène liés en utilisant le composant fluorure de bore disponible déshydratant. Son introduction dans le processus de réaction permet de réduire le coût du produit obtenu, qui met à la disposition de la nitration de toluène. processus découlant de l'équation sont généralement les suivantes:
ArH + HNO3 + BF3 = Ar-NO2 + BF3 · H2 O
Après l'achèvement de l'eau de réaction est introduit, de sorte que les formes de dihydrate de fluorure de bore monohydraté. Il a été éliminé sous vide, puis ajouter du fluorure de calcium, de retour à la forme de composé d'origine.
Spécificité de nitration
Il y a quelques caractéristiques du processus associé au choix des réactifs, le substrat en utilisant une réaction. Examinons quelques-uns de leurs plus d'options:
- 60-65 pour cent d'acide nitrique à un mélange d'acide sulfurique à 96 pour cent;
- mélange de 98% d'acide nitrique et d'acide sulfurique concentré pour la réaction de quelques substances organiques;
- le nitrate de potassium ou d'ammonium avec de l'acide sulfurique concentré, – est un excellent choix pour la production de polymères de composés nitrés.
La cinétique de nitration
des hydrocarbures aromatiques, en interaction avec un mélange d'acides sulfurique et nitrique, nitro ioniquement. V. Markovnikov capables de caractériser la spécificité de l'interaction. Le processus se déroule en plusieurs étapes. acide Nitrosernaya est d'abord formée, qui subit une dissociation en solution aqueuse. des ions nitronium sont mis à réagir avec du toluène à former en tant que nitrotoluène du produit. Lorsqu'il est ajouté à un mélange de molécules d'eau se produit lors de la décélération.
Dans des solvants organiques avec la nature – le nitrométhane, l'acétonitrile, le sulfolane – permet la formation du cation augmenter le taux de nitration.
Le cation nitronium résultant est attaché au noyau aromatique de toluène, ainsi formé intermédiaire. En outre il existe un écart de protons, ce qui conduit à la formation de nitrotoluène.
Pour une description détaillée du processus en cours, nous pouvons envisager la formation d'un complexe « sigma » et « pi ». Education « sigma » du complexe est l'étape limitante de l'interaction. La vitesse de réaction est directement liée à la rapidité de fixation du cation nitronium à l'atome de carbone dans le noyau des composés aromatiques. le fractionnement du proton hors de toluène est effectuée presque instantanément.
Seulement dans certaines situations, il peut y avoir quelques problèmes avec le remplacement associé à un effet isotopique cinétique primaire importante. Cela est dû à l'accélération du processus de retour en présence d'obstacles de divers types.
Lors de la sélection d'un catalyseur et d'un agent déshydratant avec le processus de l'acide sulfurique concentré, il est changement équilibre vers la formation de produits de réaction.
conclusion
Il a formé dans la nitration de toluène nitrotoluène, qui est un produit précieux de l'industrie chimique. Il est cette substance est un composé explosif, la demande dans les opérations de dynamitage. Parmi les problèmes environnementaux liés à sa fabrication industrielle, notez l'utilisation d'une quantité importante d'acide sulfurique concentré.
Pour faire face à ce problème, les chimistes cherchent des moyens de réduire l'acide sulfurique résiduaire obtenu après le processus de nitration. Par exemple, le procédé est mis en oeuvre à des températures plus basses, le milieu utilisé est facilement régénérable. L'acide sulfurique a des propriétés oxydantes fortes, ce qui affecte négativement la corrosion des métaux est un danger accru pour les organismes vivants. Conformément à toutes les normes de sécurité possibles pour faire face à ces problèmes, obtenir des composés nitro de haute qualité.













