Considérons la structure électronique de l'atome de fer, ainsi que sa position dans le tableau périodique. Identifier les propriétés physiques et chimiques clés de l'élément, le champ d'utilisation.
La situation dans la SS
Le fer est un groupe d-8 élément (groupe de transition). 26 a un numéro de série, la masse atomique relative – 56, dans son atome contient 26 protons, 26 électrons, et 30 neutrons. Ce métal a une réactivité élevée, présente des propriétés réductrices. état d'oxydation typique +2, +3.
Caractéristiques de la structure de l'atome
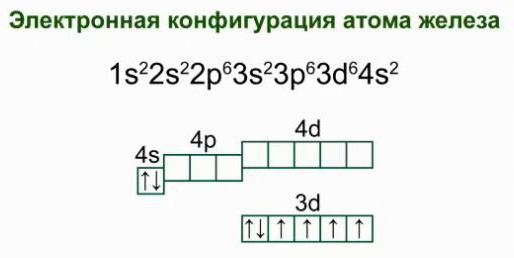
Qu'est – ce qu'un électronique schéma de la structure d'un atome de fer? Si l'on considère la répartition des électrons dans les niveaux d'énergie, on obtient le mode de réalisation suivant:
2e; 8 E; 14 e; 2e. Une telle structure de la coquille d'électrons d'un atome de fer témoigne de son emplacement dans les sous-groupes, confirme appartenant à la famille des éléments Dr..

Être dans la nature
Le fer est l'un des plus communs des éléments chimiques naturels. Dans la croûte sa teneur en pourcentage est d'environ 5,1%. En plus dans les profondeurs de notre planète, il n'y a que trois éléments: le silicium, l'aluminium, l'oxygène.
Les minerais de fer se trouvent dans différentes régions de la Terre. Alchimistes ont été trouvés composé de ce métal dans le sol. Dans la production de minerai de fer est choisi dans lesquels la teneur est supérieure à 30 pour cent.
Le fer magnétique contient environ soixante-douze pour cent du métal. dépôts de magnétite de base sont situés dans des anomalies magnétiques Koursk, ainsi que dans les montagnes du sud de l'Oural. En pourcentage Bloodstone de fer atteint 65 pour cent. Hématite a été trouvé dans la région Krivoï Rog.

La valeur des plantes et des animaux
Quel est le rôle dans les organismes vivants, effectue fer? La structure de l'atome explique ses propriétés réparatrice. Cet élément chimique fait partie de l'hémoglobine, ce qui lui donne une couleur rouge caractéristique. Environ trois grammes de fer pur, dont la plupart est incorporé dans l'hémoglobine, on trouve dans le corps d'un adulte. Le but principal est de transférer vers les tissus des poumons de l'oxygène actif et le retrait du dioxyde de carbone formé.
A besoin de ce métal et des plantes. Dans le cadre du cytoplasme, il prend une part active dans le processus de photosynthèse. Si la plante est pas assez de fer, ses feuilles ont une couleur blanche. Avec des sels dressings minimales de l'usine de fer feuilles vert.
propriétés physiques
Nous avons examiné la structure de l'atome de fer. Le circuit confirme que cet élément de lustre métallique (électrons de valence est disponible). Dans un métal blanc argenté point de fusion relativement élevé (1539 degrés Celsius). En raison de la bonne ductilité du métal peut être facilement laminage, emboutissage, forgeage.
Capacité à aimantation et caractéristique démagnétisation du fer, fait un excellent matériau pour la production de noyaux de électroaimants puissants dans différents véhicules et les voitures électriques.
Comment le fer actif? La structure montre la présence de l'atome au niveau externe des deux électrons qui seront donnés au cours d'une réaction chimique. Pour augmenter sa dureté et la force, et effectuer métal dur roulement supplémentaire. Ces processus ne sont pas accompagnés d'un changement dans la structure de l'atome.

espèces de fer
La structure électronique de l'atome de fer, le schéma qui a été discuté ci – dessus, décrit ses caractéristiques chimiques. En métal commercialement pur, qui est un acier bas carbone dont le composant principal est le fer. Comme l'impureté a révélé environ 0,04 pour cent de carbone, contient également du phosphore, de l'azote, le soufre.
fer chimiquement pur sur ses paramètres extérieurs semblables à platine. Il a une grande résistance aux processus de corrosion, stable aux acides. Aux impuretés légères sont introduites dans un métal pur ses caractéristiques uniques disparaissent.
les options pour
La structure des atomes d'aluminium et de fer appartenant amphotère indique le sous-groupe principal à l'aluminium, la possibilité de l'utiliser dans le procédé de séparation du fer à partir de ses oxydes. Aluminothermie effectuée à une température élevée, il permet d'allouer métal pur à partir de minerais naturels. En plus de l' aluminium comme agent réducteur fort est choisi un atome d' hydrogène, un oxyde de carbone (2) et le charbon.
propriétés chimiques en particulier
Quelles sont les propriétés chimiques du fer? La structure de l'atome explique son activité réductrice. Pour le fer, caractérisé par la formation de deux séries de composés possédant l'état d'oxydation +2, +3.
Dans l'air humide, il y a une rouille de traitement (corrosion) du métal, résultant en la formation d'hydroxyde de fer (3). Avec le fil de fer chauffé d'oxygène réagit avec l'arrivée de la poudre d'oxyde de fer noir (2,3), dite couche d'oxyde de fer.
A métallique à haute température capable de réagir avec la vapeur d'eau, de manière à former un oxyde mixte. Le processus est accompagné par le dégagement d'hydrogène.
La réaction avec les non-métaux se produit uniquement au chauffage préalable des composants de départ.
Le fer peut être dissous dans de l'sulfurique dilué ou l'acide chlorhydrique, sans préchauffage du mélange. sulfurique concentré et de l'acide chlorhydrique passiver le métal.
Que possède des propriétés chimiques du fer? La structure d'un atome de l'élément indique l'activité moyenne. Cette situation est confirmée fer à l'hydrogène (H2) dans la série électrochimique. Par conséquent, il peut déplacer parmi les sels de tous les métaux, qui sont situés à droite dans la rangée Beketova. Ainsi, la réaction avec du cuivre (2) est réalisée sous chauffage, est une allocation de cuivre pur et l'obtention d'une solution de chlorure ferrique (2).
 applications
applications
La majeure partie du fer total est utilisé dans la production du fer et de l'acier. Le pourcentage de fer teneur en carbone de 3-4 pour cent dans l'acier – pas plus de 1,4 pour cent. Cet élément non métallique remplit la fonction d'améliorer la résistance de liaison. En outre, il affecte positivement les propriétés de corrosion d'alliages augmente la résistance du matériau à une température élevée.
vanadium additifs nécessaires pour améliorer la résistance mécanique de l'acier. Le chrome augmente la résistance aux produits chimiques agressifs.
propriétés ferromagnétiques de cet élément chimique rendu populaire dans les applications industrielles, y compris dans les électroaimants. En outre, le fer a trouvé son utilisation dans l'industrie du souvenir. Une base pour la production de divers souvenirs tels aimants colorés sur le réfrigérateur.
La force et la ductilité permettent l'utilisation du métal pour la création d'armures, armes diverses.
chlorure de fer (3) utilisé pour la purification de l'eau des impuretés. En médecine 26 élément tableau périodique utilisé dans le traitement de maladies telles que l'anémie. En cas de pénurie de globules rouges il y a la fatigue, le teint peau un aspect anormalement pâle. préparations de fer aident à éliminer ce genre de problème, le retour du corps à des activités normales. Le fer a une importance particulière pour l'activité de la glande thyroïde, le foie. Alors que le corps humain est pas de problèmes sérieux, consommer suffisamment chaque jour environ 20 mg du métal.











