l'oxyde d'arsenic: préparation et les propriétés
Dans un tel élément de table périodique, tels que l'arsenic, il occupe une position au niveau du métal – non métallique. Par leur activité, il est entre l'hydrogène et le cuivre. nature non métallique manifeste dans le fait qu'il est en mesure d'exercer un degré d'oxydation -3 (AsH3 – arsine). Les composés ayant un état d'oxydation positif 3 ont des propriétés amphotères, et avec le degré de 5 manifestent leurs propriétés acides. Qu'est-ce que l'oxyde d'arsenic?

Oxydes et hydroxydes
Les oxydes d' arsenic suivantes: As 2 O 3 et As 2 O 5. Il y a aussi un hydroxydes correspondants:
- HAsO acide Metamyshyakovistaya 2.
- acide Ortomyshyakovistaya H 3 AsO 3.
- acide Metamyshyakovaya HAsO 3.
- acide Ortomyshyakovaya H 3 AsO 4.
- acide Piromyshyakovaya H 2 Comme 4 O 7.
Qu'est-ce que le trioxyde d'arsenic?
oxyde d' arsenic forme dont deux As 2 O 3 a le trioxyde de nom. Cette substance, qui est souvent utilisé pour le traitement, mais il est un produit chimique inoffensif. Ce composé inorganique qui est un composé de grands organoarsenicheskih source (composés contenant des liaisons carbone c) et beaucoup d'autres. Beaucoup utilisent As 2 O 3 sont controversés en raison de la toxicité de l'élément. Nom commercial de ce composé est Trisenox.
Informations générales sur trioxyde
La formule chimique de trioxyde d' arsenic a la forme suivante As 2 O 3. Le poids moléculaire du composé est 197,841 g / mol. Il y a plusieurs façons d'obtenir cet oxyde. L'un d'eux est le grillage du minerai sulfuré. La réaction chimique est la suivante:
2AS 2 O 3 + 2 → 9O 2AS 2 O 3 + 2 6SO
La plupart des oxydes peut être obtenu comme sous-produit du traitement d'autres minerais. Arsénopyrite est une impureté commune dans l'or et le cuivre, et il libère trioxyde d'arsenic, lorsqu'il est chauffé en présence d'air. Cela peut conduire à une intoxication grave.

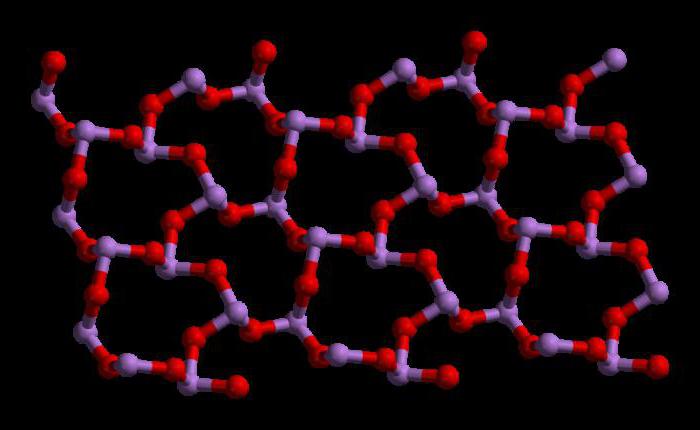
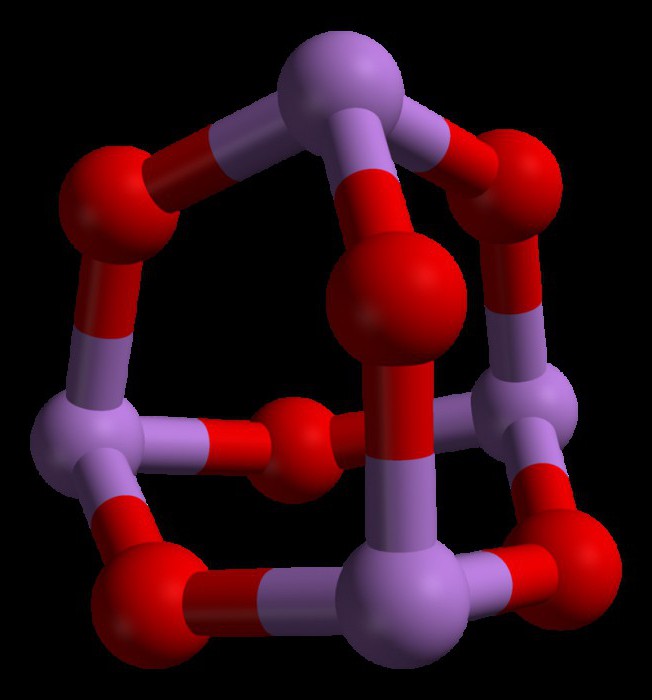
La structure du trioxyde d'arsenic
Le trioxyde d'arsenic répond à la formule As 4 O 6 dans les phases liquide et gazeuse ( en dessous de 800 ° C). Dans ces phases, il est isostructural avec du trioxyde de fosforovym (P 4 O 6). Cependant, à des températures supérieures à 800 ° C , comme 4 O 6 effondrements à moléculaire As 2 O 3. Dans cette phase , il est isostructural avec diizotrona trioxyde (N 2 O 3). Dans son état solide, ce composé présente une capacité polymorphe (capacité à exister sous deux ou plusieurs formes de structure cristalline).
Propriétés de trioxyde d'arsenic
Certaines des propriétés de base de trioxyde d'arsenic sont les suivantes:
- solutions de trioxyde forment acide faible avec de l'eau. Cela est dû au fait que le composé amphotère est un oxyde d'antimoine.
- Il est soluble dans les solutions alcalines et donne arséniate.
- le trioxyde d'arsenic a une solubilité élevée dans l'acide chlorhydrique (HCl), et fournit enfin un trichlorure d'arsenic et de l'acide concentré.
- Il pentoxyde donne (As 2 O 5) en présence d'oxydants forts tels que le peroxyde d'hydrogène, l' ozone et l' acide nitrique.
- Il est pratiquement insoluble dans les solvants organiques.
- Il ressemble à un solide blanc dans un état physique normal.
- Il a un point de fusion de 312,2 ° C et un point d'ébullition de 465 ° C
- La densité de cette matière est de 4,15 g / cm 3.
L'utilisation de trioxyde d'arsenic en médecine
Ce produit chimique est une classe d'agents antinéoplasiques, et est utilisé dans le traitement du cancer. toxicité de l'arsenic est bien connu. Cependant, le trioxyde d'arsenic est un médicament de chimiothérapie utilisé pour traiter certains types de cancer depuis de nombreuses années. La solution utilisée pour ce traitement est appelé solution Fowler. En 1878, godu Boston City Hospital a indiqué que cette solution peut être efficace pour réduire le nombre de leucocytes chez les humains.
Comme il a été utilisé principalement à la suite 2 O 3 pour le traitement de la leucémie, aussi longtemps jusqu'à ce qu'il soit remplacé la radiothérapie. Mais après les années 1930, il a progressivement retrouvé sa popularité dans le traitement de la leucémie, tant qu'il y avait une chimiothérapie moderne. Cet oxyde d'arsenic est considéré comme la meilleure méthode de traitement de la leucémie myéloïde chronique. Aujourd'hui encore, cette substance est utilisée pour traiter un type particulier de leucémie aiguë promyélocytaire avec rétinoïde échec ou la chimiothérapie anthracycline. Il est également utilisé pour traiter la leucémie myéloïde chronique, le myélome multiple, la leucémie myéloïde aiguë, le lymphome, le cancer du système lymphatique.

En utilisant trioxyde
Le trioxyde d'arsenic est largement utilisé dans la fabrication du verre incolore. Ce composé est également utile dans l'électronique pour construire des semi-conducteurs et des alliages. Il est utilisé dans les peintures. Le trioxyde d'arsenic peut être efficace dans le traitement des tumeurs cérébrales.
Dans le passé, cette substance est utilisée en médecine dentaire, mais parce qu'il est un composé très toxique, l'utilisation de la dentisterie moderne a été abandonnée. oxyde d' arsenic (As 2 O Formule 3) est également utilisé comme agent de conservation pour le bois, mais ces matériaux sont interdits dans de nombreuses régions du monde. En combinaison avec de l'acétate de cuivre de trioxyde d'arsenic donne un pigment vert clair.
substance très toxique
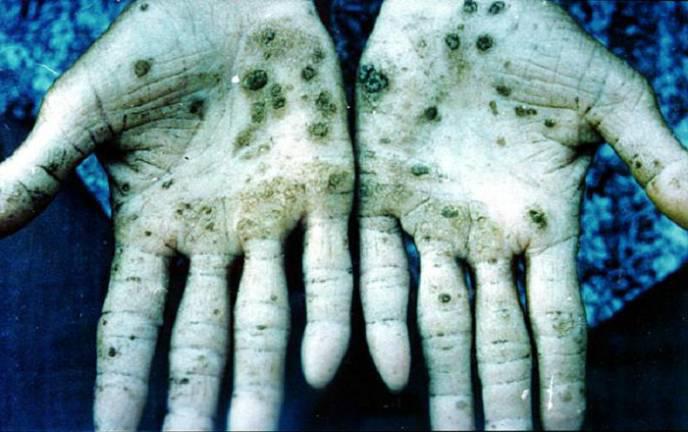
Lui-même a un Trioxyde de haut niveau de toxicité. Par conséquent, vous devez toujours prendre les précautions nécessaires avant de l'utiliser. Il peut être très dangereux dans les cas suivants:
- Repas. Si As 2 O 3, est accidentellement dans le tube digestif, vous devriez consulter immédiatement un médecin. Il est recommandé de ne pas essayer de faire vomir avant de demander une aide médicale. Il est nécessaire d'enlever les vêtements serrés, enlever sa cravate, déboutonner le col, la ceinture et ainsi de suite. D.
- Le contact avec la peau. En cas de contact avec une surface du corps doit laver immédiatement la zone affectée avec beaucoup d'eau. vêtements et chaussures contaminés doivent être retirés immédiatement, et ils doivent être lavés avant de les réutiliser. En cas de contact avec la peau grave, vous devriez consulter immédiatement un médecin. Il peut être utile pour désinfecter le lavage de la zone infectée avec du savon et de l'application de la crème anti-bactérienne.
- Contact avec les yeux. Si As 2 O 3 entre en contact avec les yeux, la première chose à faire est d'enlever les lentilles de contact et lavage des yeux avec de l' eau pendant 15 minutes. Il est recommandé d'utiliser l'eau froide. Parallèlement à cela, quelqu'un doit appeler une ambulance.
- L'inhalation. Les personnes qui ont inhalé le gaz, doivent être placés dans un autre endroit avec de l'air frais. En outre, vous devriez consulter immédiatement un médecin. Si la difficulté à respirer, l'oxygène doit être administré immédiatement. Si la victime est incapable de respirer par eux-mêmes, vous devez donner la respiration artificielle.
- Ce composé peut avoir un effet toxique sur les humains. En cas d'ingestion de quantités excessives de trioxyde d'arsenic, il peut même conduire à la mort. Des lunettes de sécurité et des gants doivent toujours être utilisés lorsque vous travaillez avec As 2 O 3. Les travaux devraient toujours être effectué dans un endroit bien ventilé.
effets secondaires
Les effets secondaires courants de cette substance comprennent des symptômes tels que:
- le manque d'appétit;
- vomissements;
- nausées;
- douleur abdominale;
- la constipation;
- maux de tête;
- fatigue;
- vertiges;
- la fièvre;
- problèmes respiratoires;
- niveau élevé de leucocytes;
- une glycémie élevée;
- éruption cutanée.
Moins d'effets secondaires communs incluent:
- sécheresse de la bouche;
- respiration incompatible;
- douleur thoracique;
- de faibles niveaux de leucocytes;
- des douleurs musculaires et des os;
- gonflement du visage et des yeux;
- diarrhée;
- tremblements;
- sucre dans le sang;
- Les faibles niveaux d'oxygène dans le sang.
Les effets indésirables rares de As 2 O 3:
- rythme cardiaque irrégulier (qui peut même conduire à la mort);
- le gain de poids;
- perte de connaissance;
- distraction;
- coma;
- ventre gonflé;
- assombrissement de la peau.
symptômes menaçant le pronostic vital de l'exposition au trioxyde d'arsenic – un gain de poids, de la fièvre, des difficultés respiratoires, essoufflement, douleur thoracique, toux.
Le trioxyde d'arsenic est une substance hautement toxique, qui peut même conduire à la perte de la vie. Néanmoins, il doit être utile dans le domaine médical. Nous devons toujours prendre des précautions.
réactions chimiques
Le trioxyde d' arsenic est un agent tensioactif amphotère oxydes supérieurs d'arsenic et ses solutions aqueuses sont faiblement acide. Ainsi, il est facilement soluble dans des solutions alcalines pour obtenir arséniates. Il est moins soluble dans les acides, sauf chlorhydrique.
Seulement avec les oxydants forts tels que l' ozone, le peroxyde d'hydrogène et d' acide nitrique, il est formé de penta-oxyde d' arsenic avec un degré d'acidité de 5 As 2 O 5. En ce qui concerne la résistance à l'oxydation, le trioxyde d'arsenic est différente de trioxyde de phosphore, qui est facilement brûlé au pentoxyde de phosphore. La réduction donne l' arsenic élémentaire ou arsine (AsH3).
pentoxyde d'arsenic
pentoxyde chimique de formule est la 2 O 5. Sa masse molaire 229.8402 g / mol. Il est une poudre hygroscopique blanche avec une densité de 4,32 g / cm 3. Point de fusion atteint 315 ° C, à laquelle il commence à se décomposer. La substance a la bonne solubilité dans l'eau et l'alcool. propriétés d'oxyde d'arsenic rendent très toxiques et dangereux pour l'environnement. Ce composé inorganique qui est une application commerciale moins fréquente, hautement toxique et trouve donc limitée uniquement, contrairement à l'oxyde d'arsenic supérieur (As 2 O Formule 3).
L'arsenic est surtout connu comme un poison et cancérigène. Son trioxyde – une poudre soluble dans l'eau, ce qui produit une solution incolore, inodore et sans saveur. Il était une méthode populaire de tuer au Moyen Age. Son utilisation se poursuit aujourd'hui, mais à des fins pacifiques et en petites quantités.